海外第Ⅲ相臨床試験(PSOR-008試験:ESTEEM-1試験)
海外第Ⅲ相臨床試験(PSOR-008試験:ESTEEM-1試験)
試験デザイン
海外第Ⅲ相臨床試験(PSOR-008試験:ESTEEM-1 試験)4-8)(海外データ)
- 【目 的】
- 中等症~重症の尋常性乾癬患者にオテズラ30mgを1日2回経口投与したときの有効性及び安全性を、プラセボを対照として評価する。
- 【対 象】
- BSA10%以上、PASIスコア12以上、sPGAスコア3以上の中等症~重症の18歳以上の尋常性乾癬患者844例
- 【方 法】
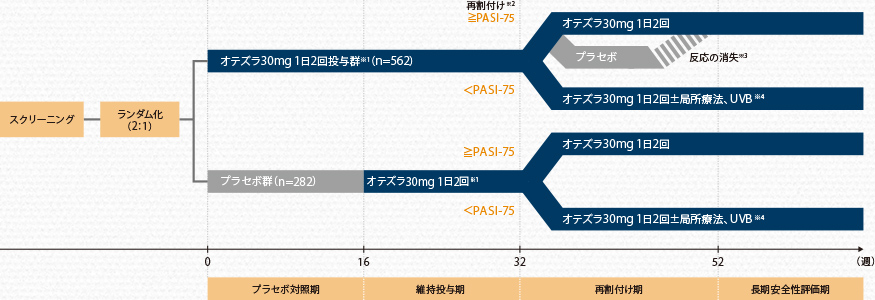
- 第Ⅲ相多施設共同、ランダム化、二重盲検、プラセボ対照試験。本試験はプラセボ対照期(16週間、ランダム化、二重盲検)、維持投与期(16週間、二重盲検)、再割付け期(20週間、ランダム化、二重盲検)及び長期安全性評価期(208週間、非盲検)の4期で構成された。
プラセボ対照期では、オテズラ30mg 1日2回投与群又はプラセボ群に2:1でランダムに割付け、16週間投与した。プラセボ群では16週時に盲検下でオテズラ30mg 1日2回投与に切り替え、オテズラ30mg 1日2回投与群では同用量を盲検下で32週まで継続した(維持投与期)。32~52週の治療中の評価は上記のとおり実施し、52週時に長期安全性評価期に移行したすべての患者はオテズラ30mgを1日2回で最長4年間投与した。
- オテズラの投与開始時又はプラセボからオテズラへの投与切り替え時は、最初の6日間にオテズラを1日あたり10mgずつ漸増投与。
- プラセボ対照期のオテズラ30mg 1日2回投与群のうち32週時にPASI-75を達成した患者をオテズラ30mg 1日2回又はプラセボ投与に再割付け。
プラセボ対照期のオテズラ30mg 1日2回投与群のうちPASI-75未達成患者、及びプラセボ対照期のプラセボ群の患者は再割付けせず、52週までオテズラ30mg 1日2回投与を継続。 - プラセボ群に再割付けされPASI-75が消失した患者は、オテズラ30mg 1日2回投与を再開。
- 32週時のPASI-75未達成患者は、治験担当医師の判断により、局所療法や紫外線B波(UVB)の光線療法の併用が可能。
- 【主要評価項目】
- 投与16週時のPASI-75達成率(検証的な解析項目)
- 【副次評価項目】
- 投与16週時のsPGA達成率、投与16週時の乾癬病変のBSA(%)のベースラインからの変化率、投与16週時のPASIスコアのベースラインからの変化率、 投与16週時のPASI-50達成率、投与16週時のそう痒VASスコアのベースラインからの変化量、投与16週時のDLQI合計スコアのベースラインからの変化量等
- 【探索的評価項目】
- 投与16週時のNAPSIスコア※5のベースラインからの変化率、投与16週時のScPGAスコア0/1達成率※6、投与24、32週時のPASIスコアの変化率、投与24、32週時のそう痒VASスコアのベースラインからの変化量、投与24、32週時のDLQI合計スコアのベースラインからの変化量等
- 【解析計画】
- 目標症例数は主要評価項目(投与16週時のPASI-75達成率)においてプラセボ群に対する差を検出できるよう設計した。
有効性の解析では、ステップダウン法を用いて統計学的に比較を行った。主要評価項目に続き、副次評価項目(上記記載順)、さらに投与16週時の探索的評価項目(上記記載順)の順に、ある評価項目がp<0.05(両側)で、かつその前の評価項目すべてが統計学的に有意(p<0.05)であった場合のみ、当該項目は統計学的に有意であるとし、ステップダウン法の階層基準を満たさなかった評価項目でp<0.05(両側)であった場合は、未調整のp値(名目上のp値)として記載した。
- NAPSI(Nail Psoriasis Severity Index)スコア:左右の指の中で最も乾癬の症状が重い爪(評価爪)の重症度を評価する指標。合計スコアが高いほど爪乾癬の重症度が高いことを示す。
- ScPGAスコア0/1達成率:頭皮の乾癬を有する患者において、頭皮に対する医師による全般評価指標であるScPGA(Scalp Physician Global Assessment)スコアが0(消失)又は1(ほぼ消失)に改善した患者の割合。
4)CC-10004-PSOR-008試験(承認年月:2016年12月、CTD2.7.6.20)(承認時評価資料)
5)Papp K et al.:J Am Acad Dermatol. 73:37-49, 2015
6)Rich P et al.:J Am Acad Dermatol. 74:134-142, 2016
7)Sobell JM et al.: Acta Derm Venereol. 96: 514-520, 2016
8)Thaçi D et al.: J Eur Acad Dermatol Venereol. 31: 498-506, 2017
利益相反:PSOR-008試験(ESTEEM-1)はAmgen社(旧 Celgene社)の資金提供によりアプレミラストの開発治験として実施され、この結果を報告した論文5)[Papp K et al.: J Am Acad Dermatol. 73: 37-49, 2015]、6)[Rich P et al.: J Am Acad Dermatol. 74: 134-142, 2016]、7)[Sobell JM et al.: Acta Derm Venereol. 96: 514-520, 2016]、8)[Thaçi D et al.: J Eur Acad Dermatol Venereol. 31: 498-506, 2017]の著者らには、Amgen社(旧 Celgene社)の社員や指導料などの謝金を受領した者を含みます。
○局所療法で効果不十分な尋常性乾癬 ○乾癬性関節炎
6. 用法及び用量
通常、成人にはアプレミラストとして以下のとおり経口投与し、6日目以降はアプレミラストとして1回30mgを1日2回、朝夕に経口投与する。
| 1日目 | 2日目 | 3日目 | 4日目 | 5日目 | 6日目以降 | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| 朝 | 朝 | 夕 | 朝 | 夕 | 朝 | 夕 | 朝 | 夕 | 朝 | 夕 |
| 10mg | 10mg | 10mg | 10mg | 20mg | 20mg | 20mg | 20mg | 30mg | 30mg | 30mg |








 海外第Ⅲ相臨床試験(PSOR-008試験:
海外第Ⅲ相臨床試験(PSOR-008試験: に ついての情報サイト
に ついての情報サイト

 でログイン
でログイン